- 首页
- 医院概况
- 党建动态
- 新闻中心
- 招标采购
- 科室导航
- 就医指南
- 护理园地
- 科研教学
- 专病中心
 2026/05/06
2026/05/06
 105
选择字号:
105
选择字号:小
中
大
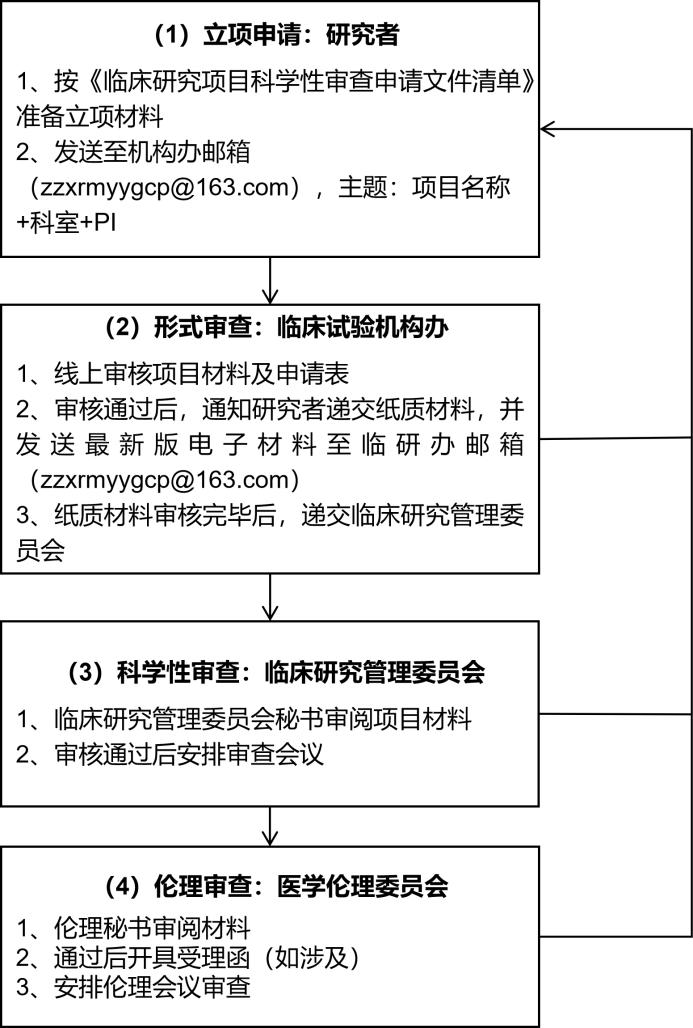
返回列表一、立项申请
研究者按项目类别,参照附件1《临床研究项目科学性审查申请文件清单》准备IIT项目材料,打包发送至机构办邮箱(zzxrmyygcp@163.com),邮件主题:项目名称+科室+PI。
二、形式审查
临床试验机构办负责对研究者递交的临床研究相关资料进行形式审查,主要审查材料的完整性和规范性,并回复审查意见:
资料主要包含临床研究方案;知情同意书、病历报告表等(详见附件1)。
三、科学性审查
1.机构办秘书形式审查通过后,转交医院临床研究管理委员会进行科学性审查。
2.科学性审查结论分五类:同意;不同意;做必要修正后同意;做必要修正后重审;终止或暂停已批准的研究。
3.结论为“同意”的,由主任委员签发《中江县人民医院临床研究立项通知》。
4.结论为“修正后同意”的,书面告知研究者;修改后经快速审查通过,由主任委员签发《中江县人民医院临床研究立项通知》。
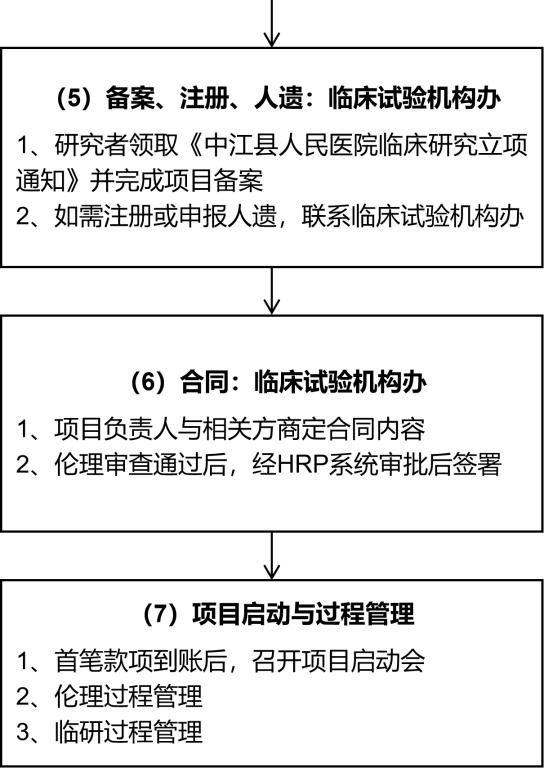
四、医学研究登记备案
项目通过伦理审查并获得伦理批件后,在项目启动前登录国家医学研究登记备案信息系统(https://www.medicalresearch.org.cn/login)完成备案。多中心研究由组长单位备案,参与单位无需重复备案。
五、人遗申报(如需)
涉及人类遗传资源采集、保藏、利用、对外提供等的研究,须获国务院科技行政部门批准后方可开展。如需申报,请联系临床试验机构办。
六、研究项目合同
研究者发起的课题由临床试验机构办按医院合同模板管理。与外单位合作的均须以医院名义签订合同。伦理审查通过后,项目负责人应将商定后的合同提交HRP系统审批,签署正式合同。
七、联络方式
临床试验机构办公室:0838-7237012
伦理委员会办公室:0838-7210829
八、附件
附件1 临床研究项目科学性审查申请文件清单
附件2 立项资料
附件3 结题资料
附件4 合同模板
立项流程
上一条 2026-05-06
GCP项目资料递交指南下一条 2026-04-27
招募!支气管哮喘受试者 - 党建动态















